酵素を模倣した金属-硫黄化合物により窒素還元反応を実現 ―持続可能社会に寄与するエネルギー変換に向けた第一歩―
京都大学化学研究所 大木靖弘 教授、松岡優音 同大学院生、谷藤一樹 同助教らは、名古屋大学 唯美津木教授、ハワイ大学 Roger E. Cramer 教授、コロンボ大学 W. M. C. Sameera准教授、大同大学 高山努 教授、酒井陽一 同教授、東京大学 西林仁昭 教授、栗山翔吾 同助教らと共同で、自然界の触媒(酵素)を模倣する金属-硫黄クラスター錯体を合成し、窒素分子(N2)の還元反応(シリル化反応)を実現しました。
大気の主成分であるN2の化学変換は、アミノ酸やDNAに含まれる窒素原子を供給するために必要な一方で、非常に難しい反応として知られています。自然界では、一部の微生物に存在する酵素ニトロゲナーゼだけがこの役割を担い、Fe-Mo-S-Cから構成される酵素活性中心(FeMoco)を用いてN2を還元します。FeMocoの触媒機能は、持続可能社会に向けた新しいN2還元法を開発する重要なヒントになりますが、複雑なFeMocoは構造と機能の関係を理解するのが難しく、またタンパク質から取り出すと触媒機能を失います。FeMocoに関連する従来の金属-硫黄化合物もN2を還元できなかったことから、N2還元作用の鍵となる要素は未解明のままでした。本研究では、N2が結合したFeMocoの予想構造およびタンパク質の一部機能を模した[Mo3S4Fe]錯体を合成し、これを触媒としてN2の還元反応を達成しました。この結果は、金属-硫黄化合物の可能性を切り拓くと同時に、自然界に学び、超えるための大きな第一歩といえます。
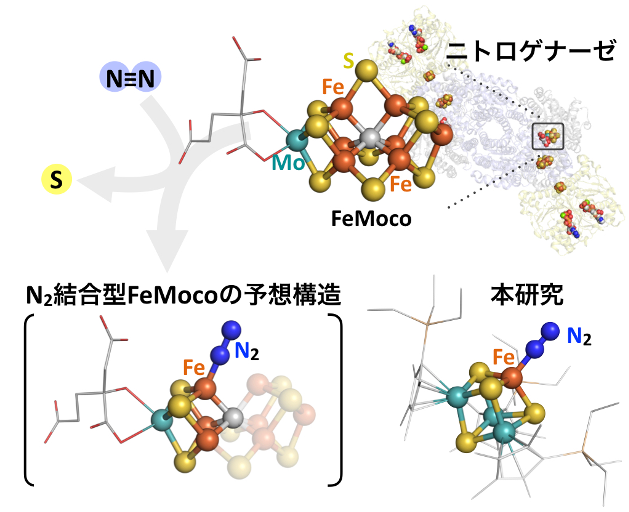
大気中の窒素分子(N2)をアンモニア(NH3)等の生物が利用できる分子へ変換する窒素固定(N2還元反応)は、アミノ酸やDNAに含まれる窒素原子を供給し、生命活動を維持する上で欠かせません。その一方で、強いN≡N三重結合を持つ対称構造のN2は、不活性ガスと呼ばれるほど反応性に乏しいため、N2の還元は非常に難しい反応として知られています。自然界では、一部の微生物に存在する酵素ニトロゲナーゼがN2還元反応を担いますが、この自然界での反応だけでは地球上の人口の食糧生産を支えられるほどの窒素量を賄えません。そのため、鉄やルテニウムを触媒とする工業反応であるハーバー・ボッシュ法により、N2と水素分子(H2)から高温高圧条件下でNH3が合成されています。この工業反応には、人類が使う全エネルギーの1〜2%が費やされ、また同時にH2の原料として化石燃料を消費し、大量のCO2を発生します。化石燃料に頼らない酵素反応を人工的に再現できれば、持続可能社会に向けた新しいN2還元技術を提供できることから、鉄(Fe)、モリブデン(Mo)、硫黄(S)、炭素(C)から構成されFeMocoと呼ばれる酵素活性中心(図1上)の働きを理解し、構造や機能を再現しようと、長年試みられてきました。しかし金属原子と硫黄原子が三次元的に配列されているFeMocoの構造は複雑なため、N2還元機能との関係を解釈するのは難しく、加えてFeMocoによるN2の還元はタンパク質に保護された状態でのみ起こることや、金属と硫黄から合成された従来のFeMoco関連分子(金属-硫黄クラスター錯体)がN2を還元できなかったことも、N2還元機能の謎を解き人工的に再現するためのハードルとなっていました。
研究グループは、酵素に関する生化学分野の知見を精査した上で、(1)どのようにN2がFeMocoへ結合するのか、(2)なぜタンパク質に保護されなければFeMocoがN2を還元しないのか、の2つの問いについて、化学の視点から仮説を導き、条件を満たす人工分子(金属-硫黄クラスター錯体)を設計・合成しようと考えました。
N2がFeMocoのどこに結合するのか、明確な答えは得られていませんが、生化学分野の知見を総括すると、FeMocoの中央部で2つのFeを架橋するS原子の1つを取り除き、その結果Feに生じる空き(反応点)がN2を取り込むと考えるのが合理的です。しかし、図1左下に示した予想構造を完璧な形で合成するのは容易ではないため、まずは大胆に簡略化して予想構造の左半分に着目し、Mo、Fe、Sを含む立方体構造のFeでN2を捕捉することにしました。なお、N2は対称構造を好むため、例えばMという金属に取り込まれるとM-N2-Mのように2つの金属原子を架橋する傾向があり、その結果N原子が2つとも金属Mに覆われて、望むN2変換反応が起こりにくくなります。従ってN2が架橋したFe-N2-Fe構造ではなく、末端のN原子が空いたFe-N2構造を作ることも重要です。これらの設計指針と構造要件、およびタンパク質の一部機能を念頭に置いて、次に注目したポイントは、凝集です。
例えば溶液中にFeとSが共存する場合、これらが容易に結合して硫化鉄(FeS)になり沈殿することは、高校化学等を通して良く知られています。同様に、タンパク質という保護枠を持たない剥き身のFeMocoは、分子間で容易に金属-硫黄結合を作り、凝集すると予想できます。しかしこの凝集は、N2還元機能を実現する上で致命的な欠点になります。なぜなら、Fe等の金属に生じる空き(反応点)がなければ反応性に乏しいN2を取り込めない一方で、別の分子に含まれる硫黄原子が反応点に接近できる場合は、金属に取り込まれたN2を硫黄が追い出して強い金属-硫黄結合を新たに形成し、反応点を塞いでしまうからです。自然界では、タンパク質の奥深くにFeMocoを埋めることで、凝集の問題を回避していると考えられます。
以上を踏まえつつ、FeMocoを模倣する分子として、Feを反応点とする立方体型の[Mo3S4Fe]クラスター錯体を設計し、さらに凝集を抑制するために、3つのMo上にかさ高いシクロペンタジエニル(CpR)配位子(CpR = C5Me5 (Cp*), C5Me4SiMe3 (CpL), C5Me4SiEt3 (CpXL); Me = CH3, Et = CH2CH3)を組み込みました。設計指針に沿って合成した[Mo3S4Fe]クラスター錯体を、大気圧のN2を満たしたフラスコ内で還元したところ、FeにN2が結合したクラスター錯体が得られました(図1右下)。このときN2の結合様式はCpR配位子により変化し、Cp*配位子を用いた場合にはFe-N2-Fe構造が、よりかさ高いCpL、CpXL配位子を用いた場合には末端Fe-N2構造が生成することを、分子構造や分光学的測定から確認しました。
続いて研究グループは、一連の[Mo3S4Fe]クラスター錯体を触媒として用い、N2の還元反応を検討しました。NH3の合成反応は効率よく進行しなかったものの、溶液で行うN2還元反応の一種であるトリス(トリメチルシリル)アミン(N(SiMe3)3)への変換反応は高効率に進行し(図2)、Fe原子当たり最大248当量のN(SiMe3)3が生成することが明らかとなりました。今回達成した触媒回転数は、Fe錯体を用いた従来の記録を3倍以上に更新しました。また、遷移金属を持つ錯体全般へと比較対象を広げても、本研究の触媒回転数はコバルト(Co)錯体やMo錯体を用いて報告されている最高値と同程度でした。
以上の結果が示す通り、今回グループが報告した[Mo3S4Fe]クラスター錯体は、FeMocoによるN2還元作用の鍵となる要素を、簡略化しつつ反映していることが分かります。人工の金属-硫黄化合物によるN2還元反応の第一歩を踏み出しただけでなく、酵素に学びつつ適切な分子設計を施すことで、金属-硫黄化合物が持つ可能性を広げられることを示す好例でもあります。
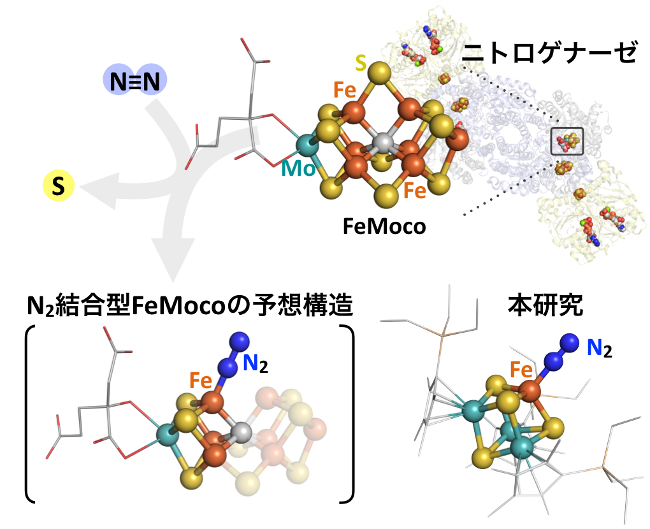
(上)酵素ニトロゲナーゼのタンパク質とFeMoco(酵素活性中心)の構造、(左下)FeMocoの窒素結合状態に関する研究グループの予想、(右下)簡略化しつつ模倣した本研究の金属-硫黄クラスター錯体。
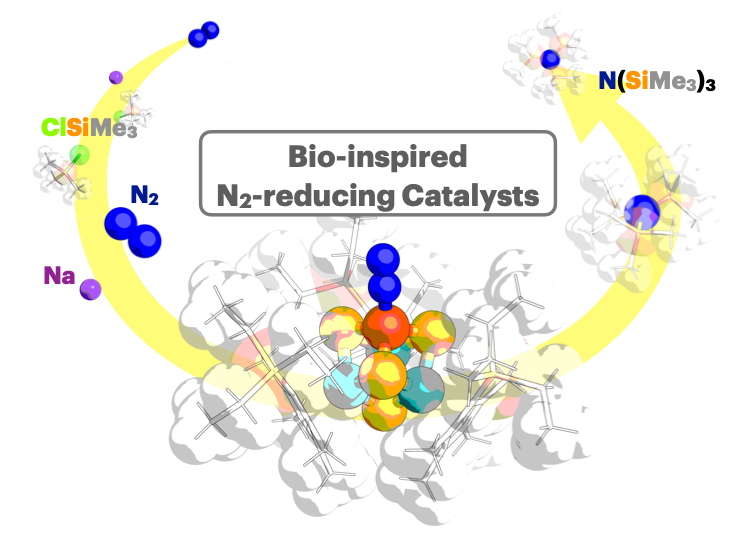
[Mo3S4Fe]クラスター錯体(中央下)の溶液を、N2で満たしたフラスコに入れ、金属ナトリウム(Na)とクロロトリメチルシラン(ClSiMe3)を加えると、N2が還元されてトリス(トリメチルシリル)アミン(N(SiMe3)3)が生成する。
以上のように研究グループは、窒素固定を担う複雑な酵素活性中心FeMocoの構造とN2還元機能の関係やタンパク質の一部機能を予想し、それらの要点を大胆に簡略化しつつ分子設計に反映することで、金属-硫黄化合物によるN2の還元に初めて成功しました。しかし、今回の成果は第一歩に過ぎません。今後、図1左下に示した予想構造を簡略化せずに合成し、N2還元反応に最適な金属元素を探索することで、酵素を超える触媒活性を実現できれば、持続可能社会に寄与する新しいN2還元法が現実味を帯びると期待しています。
本研究は、以下の研究プロジェクトの助成を受けて推進しました:JST CREST (JPMJCR21B1)、JSPS科学研究費補助金(19H02733, 20K21207, 21H00021, 21K20557)、武田科学振興財団、立松財団、矢崎科学技術振興記念財団、京都大学化学研究所 国際共同利用・共同研究拠点補助金、京都大学若手研究者スタートアップ支援
●用語解説●
錯体:ここでは、遷移金属(周期表の下部中央に見られる重金属元素)を含む分子性化合物の総称。
金属-硫黄クラスター錯体:複数の遷移金属(例えばMとする)と硫黄(S)を有する分子性化合物をまとめて呼ぶ総称。立方体型の[M4S4]構造を持つものがよく知られており、本研究で用いた[Mo3S4Fe]クラスター錯体もこれに含まれる。またFeMocoの構造は、複雑ではあるものの立方体を2つ連結したものと見ることができる
酵素活性中心:自然界の触媒(酵素)において、物質変換反応が行われる部位を指す。酵素を構成するタンパク質は巨大分子であるが、物質変換反応に直接関わる部位は、そのごく一部である。
配位子:金属と結合し、分子性化合物(錯体)を生じる物質の総称。卑近な例では水分子も配位子として働き得る。本研究では、5つの炭素原子が環状に並んだシクロペンタジエニル配位子を用いた。この配位子は、Moと強く結合して外れにくく、また比較的容易に化学修飾できるため、金属-硫黄クラスター錯体を立体的に保護する目的で導入している。
 京都大学 化学研究所
京都大学 化学研究所 国際共同利用・共同研究拠点
国際共同利用・共同研究拠点