高強度テラヘルツ光パルス照射によって変化するヒトiPS細胞内の遺伝子ネットワークの発見
iPS細胞操作技術に新しい「光」を!
化学研究所 廣理英基 准教授(兼:アイセムス 連携准教授)、京都大学 アイセムス亀井謙一郎 准教授、工学研究科 坂口怜子 助教(兼:アイセムス 連携助教)、東海大学の立崎武弘 講師(兼:アイセムス 客員講師)らの研究グループは、高強度のテラヘルツ光パルスをヒトiPSに照射すると、細胞の中で発現量が変化する遺伝子ネットワークが存在することを発見しました。iPS細胞はあらゆる細胞に分化する可能性を持った多能性幹細胞で、再生医療や創薬への応用が研究されていますが、望みの機能を持つ細胞に自在に変化させるための引き金となる遺伝子発現を制御する技術は確立されていません。
一方で、近年、高強度テラヘルツ光パルスの照射により、細胞の応答が変化する現象が報告され注目されています。しかし、その応答の変化を引き起こす機構はあまり理解されていませんでした。本研究では、世界最高レベルの強度を持つテラヘルツパルスをiPS細胞に照射し、照射の有無による細胞内の遺伝子発現の量の変化を網羅的に解析したところ、発現が亢進する遺伝子ネットワークと抑制される遺伝子ネットワークが存在することを初めて発見しました。さらに、発現が変化した遺伝子の上流では亜鉛イオン依存的な転写因子が多数存在することを突き止めました。本研究によって、高強度テラヘルツパルスを細胞に照射することで、細胞に接触せず、損傷を与えずに細胞内の遺伝子の発現パターンを変化させることができることがわかり、テラヘルツパルスで多能性幹細胞の運命を自在に操作する技術の開発につながると期待されます。
iPS細胞は2006年に最初に報告された多能性幹細胞で、再生医療や創薬技術の開発に重要な役割を果たすと期待されています。多能性幹細胞は私たちの体を構成する様々な機能を持つ細胞に分化する可能性を持っていることから、iPS細胞から分化誘導した神経細胞や肝臓などを移植する細胞移植治療への応用が研究されています。このため、近年、iPS細胞を望みの機能を持った細胞に自在に分化させる制御技術の研究が精力的に行われています。一方、電場が生体応答を制御することは古くから知られており、これまで電極を細胞に直接接触させて細胞の応答の変化を調べるという研究が行われてきました。本研究では、このような電極を用いずに高強度テラヘルツ光パルスの発生技術を活用し、非接触で瞬間的に非常に強いテラヘルツ光の持つ電場をiPS細胞内部に印加し、このときに遺伝子ネットワークに及ぼす影響について研究を行いました。
本研究では、世界最高レベルのテラヘルツ光パルスを照射することが可能で、またiPS細胞をpHや温度などの最適条件で長時間培養することができる設備を組み合わせた装置を新たに開発しました。
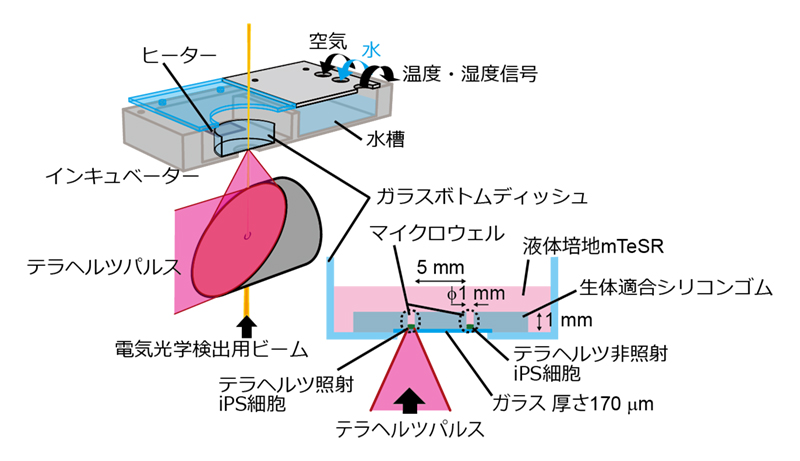
本研究は、iPS細胞の遺伝子発現ネットワークを、テラヘルツ光パルスの照射によって非接触・非侵襲的に変化させることができることを示した世界初の研究成果です。
今回の研究では、高強度テラヘルツ光パルスの電場をiPS細胞に照射することにより、細胞内で発現が変化する遺伝子ネットワークが存在することを発見しました。また、これらの遺伝子ネットワークを発現させる引き金として、亜鉛イオンによって活性化する転写因子が多数存在することも見出しました。本研究成果は、iPS細胞の遺伝子発現を、従来の成長因子などの化学的な刺激だけでなく、電場という物理的な刺激によってコントロールできる可能性を強く示唆するものです。今後、多能性幹細胞を望みの機能を持った細胞に自在に分化させる技術開発への貢献も期待されます。
本研究は、下記の助成⾦の⽀援を受けて⾏われました。
日本学術振興会(JSPS) 科学研究費補助金 挑戦的研究(開拓)(研究番号:17H06228)、基盤研究B(研究番号:17H02083、18H01140、19H02562)
国立研究開発法人科学技術振興機構(JST) 戦略的創造研究推進事業 個人型研究さきがけ(研究番号:JPMJPR1427)
●用語解説●
テラヘルツ光:テラヘルツ(電磁波)とは光波と電波の中間の周波数帯に位置する電磁波のこと。著者の研究グループは、世界最高強度のテラヘルツパルス光源の開発にも成功している。ここでの技術の蓄積が本研究に用いる複雑な装置の設計・開発に大きく貢献しています。
iPS細胞:2006年に報告された、人工多能性幹細胞。様々な組織や臓器の細胞に分化する能力をもつ細胞。
遺伝子発現:細胞外からの刺激や外環境に応じて、細胞が必要なタンパク質をつくること。
遺伝子ネットワーク:互いに協力して働くタンパク質分子の集合体のネットワーク。
転写因子:細胞が必要なタンパク質をつくるために、その設計図である遺伝子を読み出す引き金になる分子。
RNA:リボ核酸。DNAと並んで、細胞の構成要素の一種。特定の組み合わせで、タンパク質の設計図としても働く。
メッセンジャーRNA:細胞が必要なタンパク質を作るための設計図。
RNA-seq:細胞集団中に発現している遺伝子(メッセンジャーRNA)を定量的に解析する技術。
ジンクフィンガー:亜鉛イオンと結合することによって転写因子としての能力を獲得する分子。
細胞内における金属イオン:それぞれ決まったタンパク質と結合することで、そのタンパク質の機能を調節している。Ca2+, Mg2+, Zn2+が代表例。
 京都大学 化学研究所
京都大学 化学研究所 国際共同利用・共同研究拠点
国際共同利用・共同研究拠点